Apostilas sobre os nêutrons.
A radiação beta: elétrons cuspidos por núcleos. A previsão de Ernest Rutherford.
Confio que você tenha lido minhas apostilas anteriores onde contei que Ernest Rutherford descobriu três tipos de radiação provenientes de núcleos de isótopos radioativos.
(Veja A radioatividade e o decaimento do núcleo.)
1) Raios alfa (a), que hoje se sabe que são formados de dois prótons e dois nêutrons, isto é, são núcleos do elemento hélio. Têm carga elétrica positiva (+2).
2) Raios beta (b), que são elétrons (cargas negativas) de alta velocidade.
3) Raios gama (g), que são apenas radiação eletromagnética, isto é, da mesma família de nossa querida luz visível, só que muito mais penetrante e energética.

Experiência “gedanken” com radiações.
Essa figura mostra uma experiência imaginária com uma fonte hipotética desses três tipos de radiação. No real, um isótopo só irradia um dos três tipos, mas nada impede que a gente imagine um que irradie as três. Colocando placas eletricamente carregadas na saída das radiações, vemos que as partículas alfa se desviam na direção da placa negativa, as betas na direção da placa positiva e os raios gama não se desviam. Medindo os desvios das alfas e betas, pode-se calcular as massas dessas partículas.
Desses três tipos de radiação, eu, particularmente, acho que a mais interessante é a beta. Qualquer dia desses contarei a história da descoberta e interpretação dessa radiação pois é repleta de fatos curiosos. Por enquanto, basta que lhe diga que o pessoal ficou surpreso ao descobrir que elétrons eram cuspidos por alguns núcleos radioativos. Então, existem elétrons dentro dos núcleos? – eles se indagaram. Ótimo, alguns disseram, pois isso resolveria uma questão que estava pendente. Veja, por exemplo, o caso do núcleo de carbono. O carbono tem peso 12 mas a carga elétrica (6) indica que só existem 6 prótons no seu núcleo. Agora está resolvido, disseram os apressadinhos: o núcleo do carbono tem 12 prótons e 6 elétrons. Isso baixa a carga para 6 e mantém o peso em pouco mais de 12.
Essa era uma explicação atraente mas, logo, logo, Niels Bohr mostrou que estava errada. Bohr calculou as energias que os elétrons deveriam ter se fossem confinados no apertado espaço de um núcleo. Um cálculo simples de teoria quântica (que Bohr fez sem dificuldade) mostrou que um elétron dentro de um núcleo deveria ter energias da ordem de bilhões de elétrons-volt. (O elétron-volt é uma unidade de energia muito usada em Física Atômica e Nuclear). Só que as partículas beta tinham energia bem menores, da ordem de apenas uns poucos milhões de elétrons-volts. Não dava para manter um elétron tão nervoso dentro de um núcleo por muito tempo.

Ernest Rutherford.
Rutherford, então, fez outra hipótese: o núcleo conteria, além de prótons, outras partículas com peso semelhante ao dos prótons, mas, sem carga elétrica. Segundo o palpite do neo-zelandês, essa partícula neutra seria híbrida, composta da associação íntima de um próton com um elétron. O núcleo do carbono, por exemplo, conteria 6 prótons e 6 partículas neutras. A radiação de uma beta aconteceria quando essa partícula neutra se rompesse em um próton e um elétron – e, como o elétron não fica quieto dentro de um núcleo, seria cuspido para fora. O núcleo, nesse processo, teria sua carga aumentada de uma unidade e passaria a ser o núcleo de outro elemento.
Começou, então, em vários laboratórios da Europa, a busca por evidências dessa tal partícula neutra prevista por Rutherford, inicialmente sem sucesso. E, como vou contar mais adiante, foi um colaborador do próprio Rutherford que “descobriu” a partícula neutra do núcleo, depois de algumas vaciladas de outros físicos.
Mas, antes, na próxima apostila, apresentarei a vocês alguns dos heróis dessa aventura científica.
Irene e Frederico Joliot-Curie, na França, e James Chadwick, na Inglaterra.
Irene Joliot-Curie foi uma mulher extraordinária e, no entanto, pouca gente conhece sua história, talvez porque seu nome foi ofuscado pelo brilho de sua famosa mãe, Maria Curie. Tenho para mim, no entanto, que o talento da filha era parelho do da mãe, sendo que Irene era mais bela e elegante, além de ser uma corajosa socialista que desafiou os fascistas da Alemanha e dos Estados Unidos.

Irene Joliot-Curie
Maria Curie teve duas filhas, Irene e Eva. Quando as conhecí, na Paris dos anos 30, eram duas belas jovens com uma diferença: Eva era uma intelectual vaidosa e um pouco fútil, enquanto Irene, de porte naturalmente elegante, era uma cientista compenetrada e trabalhadora que, como a mãe, preferia se vestir com sobriedade.

Frederico Joliot-Curie
Já seu marido e colaborador, Frederico Joliot, era um homem charmoso, de boa conversa, tão competente quanto a mulher. Os dois se conheceram quando Frederico, por indicação de seu orientador Paul Langevin, foi trabalhar no laboratório de Maria Curie, onde Irene já era uma assistente graduada. Se foi amor à primeira vista eu não sei. Só sei que, quando se casaram, Irene adotou o sobrenome do noivo, o que é natural, e Frederico adotou o sobrenome da noiva, fato incomum mas, a meu ver, bem romântico.
Frederico, seguindo os passos de seu ex-orientador, Paul Langevin, era comunista e colaborou com a resistência francesa durante a ocupação alemã. Irene passou alguns anos da guerra em um hospital na Suiça, tratando-se de uma tuberculose. Em 1943, ao tentar entrar clandestinamente na França, foi presa e teve de passar um tempo em um campo de refugiados. Após a guerra, a penicilina já disponível, recuperou a saúde e voltou às atividades científicas e políticas. Em 1948 foi detida ao chegar aos Estados Unidos onde pretendia pedir ajuda para refugiados espanhóis, vítimas de Franco. Novamente, teve de passar uns dias em um campo de prisioneiros até que a embaixada francesa conseguiu retorná-la à França.
Irene e Frederico Joliot-Curie ganharam o prêmio Nobel de Química de 1935 por terem sidos os primeiros a sintetizar isótopos radioativos. Irene, além de suas qualidades científicas e políticas, era uma competente administradora. Foi diretora do Instituto do Radium, sucedendo sua mãe, e fez parte da Comissão de Energia Atômica do governo francês.
Assim mesmo, nunca foi aceita na Academia de Ciência da França. Os membros dessa ridícula academia, velhos machistas, não aceitavam mulheres como colegas. Nem Maria Curie, apesar de toda sua fama, venerada por todo o mundo, foi aceita. Esses franceses…
Irene morreu em 1956 de leucemia, a mesma causa da morte de sua mãe. Provavelmente, ambas foram vitimas das longas exposições a radiação. Frederico morreu dois anos depois e foi enterrado como herói de seu país.
James Chadwick

James Chadwick
O inglês James Chadwick queria ser matemático mas, quando foi fazer o vestibular entrou, por engano, na fila dos candidatos ao curso de Física. Por timidez, não trocou de fila e acabou se formando em Física, tirando a sorte grande, pois, anos depois receberia o prêmio Nobel.
Em 1913, depois de receber seu grau de Mestre, Chadwick foi trabalhar na Alemanha com Hans Geiger, aquele que inventou o famoso contador de radiação. Quando estourou a Primeira Grande Guerra foi imediatamente preso e passou todo o conflito em um campo de prisioneiros. Logo que a guerra acabou voltou ligeirinho (e meio adoentado) para a Inglaterra onde teve a sorte de trabalhar com o grande Ernest Rutherford, descobridor do núcleo atômico.
Rutherford achava que os núcleos deveriam conter, além dos prótons eletricamente positivos, partículas neutras que seriam uma combinação de prótons e elétrons. Chadwick se empenhou na busca por essas partículas até que, em 1932, com uma série de experiências muito bem elaboradas, achou o que procurava. Com sua modéstia e timidez características, publicou um artigo de meia página na revista Nature intitulado “Possível existência de um nêutron”. Esse pequeno artigo rendeu-lhe o prêmio Nobel de Física de 1935, mesmo ano em que os Joliot-Curie ganharam o prêmio de Química.
Esse será o assunto das próximas apostilas. Como você verá, o caminho até a “descoberta” do nêutron por Chadwick foi cheio de desvios e enganos. Ótimo exemplo para ilustrar a forma tortuosa como costumam ser feitos os progressos da ciência.
As experiências do casal Joliot-Curie com uma enigmática radiação neutra.
A sucessão de idas e vindas que culminou com a descoberta do nêutron começou em 1928 com algumas experiências dos alemães Walter Bothe e seu aluno Herbert Becker. Eles usavam uma amostra radioativa que produzia partículas alfa. Essas partículas alfa, como vocês lembram, têm carga elétrica positiva (+2) e são muito energéticas. Hoje sabemos que elas são idênticas aos núcleos do elemento hélio, com dois prótons e dois nêutrons. Em 1928, porém, ninguém ainda fora apresentado ao nêutron.

Walter Bothe
Bothe e Becker usavam as alfas para alvejar (ou “bombardear”, como dizem os físicos) uma amostra de berílio, metal branco, leve e muito tóxico. Notaram, então, que o bombardeio das alfas produzia um novo tipo de radiação a partir do berílio. Logo, verificaram que essa radiação era eletricamente neutra, isto é, não se desviava na presença de cargas elétricas ou ímãs. Seguindo a lei do menor esforço, concluíram que essa radiação devia ser de raios gama. Como você lembra, raios gama são ondas eletromagnéticas, como a luz visível.
Frederico e Irene Joliot-Curie leram o artigo dos alemães e resolveram reproduzir a experiância. Eles dispunham de fontes mais poderosas de partículas alfa, as amostras de polônio purificadas pela mãe de Irene, Maria Curie. Nesse reprodução da experiência, observaram também o surgimento de uma radiação neutra partindo do berílio alvejado pelas alfas e foram na onda dos alemães admitindo que era radiação gama.
Assim mesmo, foram mais adiante e, por alguma razão, resolveram usar essa radiação neutra para bombardear uma placa de parafina. O arranjo da experiência era mais ou menos o seguinte:
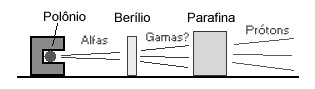
Com esse arranjo observaram que a radiação neutra desconhecida (que julgavam ser raios gama) arrancava prótons da parafina. Prótons, cargas positivas, são fáceis de serem identificados. Deu até para medir a velocidade média com que os prótons deixavam a parafina: cerca de 3,3 x 107 m/s.
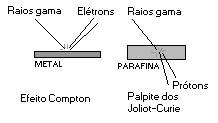
Foi nessa hora que o simpático casal comeu mosca. Para explicar como prótons eram arrancados da parafina pelos supostos raios gama fizeram um paralelo com o conhecido “efeito Compton”, descoberto anteriormente pelo americano Arthur Compton. No efeito Compton raios gama arrancam elétrons ao incidirem na superfície de um metal. De forma idêntica, eles pensaram, a radiação gama deve arrancar prótons da parafina.
O erro do casal foi não levar em conta que um próton é quase 2000 vezes mais pesado que um elétron. Raios gama podem ter energia para mover elétrons mas, dificilmente, conseguirão acelerar prótons. Minha impressão é que, nessa época, o casal estava muito concentrado em um trabalho mais empolgante: produzir isótopos radioativos artificiais. Não analisaram bem suas observações com a radiação do berílio e suas possíveis implicações. Perderam, por esse descuido, o Prêmio Nobel de Física. Tudo bem, pois ganharam o de Química com a radioatividade artificial. Só que, como veremos mais adiante, o casal ainda passaria por situação semelhante outra vez.
Como James Chadwick descobriu o nêutron

Ernest Rutherford
Quando James Chadwick relatou a Rutherford a experiência de Irene e Frederico Joliot-Curie e a explicação dada pelo casal segundo a qual a radiação do berílio seria constituída de raios gama, o velho neo-zelandês disse logo: “não acredito nisso”. Como sua enorme expreiência em colisões de partículas sub-atômicas, Rutherford desconfiou que raios gama não teriam energia suficiente para arrancar prótons da parafina. Chadwick resolveu, então, reproduzir as experiências de Bothe e dos Joliot-Curie. Acho que ele já deveria ter uma idéia pre-concebida: a radiação desconhecida que saía do berílio poderia ser feita das partículas neutras previstas por Rutherford.
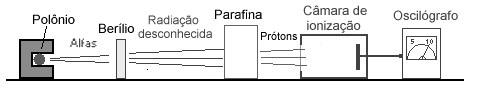
A seguir, vou descrever, com alguma licença poética, as experiências feitas por Chadwick. Do ponto de vista didático, é um ótimo exemplo de como eram feitas as pesquisas experimentais na física das partículas sub-atômicas , antes do advento dos paquidérmicos aceleradores de hoje em dia. O arranjo experimental montado por Chadwick, seguindo os passos de Bothe, era esquematicamente o seguinte:

A fonte radioativa de polônio emite partículas alfa que incidem sobre um disco de berílio. O berílio bombardeado pelas alfas produz uma radiação neutra desconhecida. Para descobrir a natureza dessa radiação, Chadwick captou-a em uma câmara de ionização. Como o nome indica, a passagem da radiação pela câmara ioniza átomos de um gás que serão, então, capturados por uma placa metálica eletricamente carregada. Desse modo, pulsos corrente saem da placa e produzem deflexões no ponteiro de um oscilógrafo. Chadwick observou que, colocando a fonte de radiação bem junto do detetor, já surgiam 4 deflexões por minuto no oscilógrafo.
Essa contagem se mantinha mesmo quando uma chapa de chumbo com 2 centímetros de espessura era colocada entre o berílio e o detetor, demonstrando que a radiação desconhecida era bastante penetrante.
A seguir, observou que, colocando uma placa de parafina entre o berílio e o detetor, as contagens no oscilógrafo aumentavam para cerca de 10 por minuto.
Isso indicava claramente que a radiação desconecida induzia a produção de outro tipo de radiação a partir da parafina. Alguns teste simples logo mostraram que essa nova radiação era formada de prótons. Chadwick conseguiu medir a energia desses prótons e logo ficou claro que eles não poderiam ser produzidos por raios gama. Uma comparação elementar utilizando a conservação da energia em um choque frontal entre partículas mostrou que uma radiação gama não seria capaz de arrancar prótons da parafina com a energia observada.
Foi então que Chadwick supôs que a radiação fosse composta de partículas neutras com peso semelhante ao peso do próton. Levando em conta essa hipótese, Chadwick usou a radiação neutra do berílio para bombardear vários gases diferentes. Desse modo, medindo a energia dos átomos desses gases após serem atingidos pela radiação, conseguiu calcular a massa das partículas neutras. Obteve um valor um pouco maior que a massa do próton, como era de se esperar.
Veja você: Bothe e Becker bolaram o arranjo experimental eproduziram o feixe de nêutrons saindo do berilio, os Joliot-Curie usaram esses nêutrons para arrancar prótons da parafina, mas, foi Chadwick, finalmente, quem mostrou com clareza a identidade desses nêutrons. Esse fenômeno pelo qual um fato importante passa por baixo do nariz de um cientista e não é adequadamente observado ou compreendido é mais comum do que se imagina. Lembre-se disso quando se tornar uma pesquisadora como Irene Joliot-Curie.
Resta dizer que a hipótese de Rutherford, segundo a qual o nêutron era uma partícula composta, mistura de próton com elétron, foi descartada rapidamente. Werner Heisenberg, famoso físico alemão de quem falarei em outra oportunidade, mostrou que o nêutron era uma partícula inteira, com o mesmo status do próton. E, tão logo foi descoberto, o nêutron se converteu em uma excelente ferramenta de pesquisa dos físicos nucleares. É o que contarei na próxima apostila.
As conseqüências da descoberta do nêutron: mais tiros no escuro.
Depois que o nêutron foi apresentado ao mundo por James Chadwick, ficou claro que essa partícula era ótima para explorar as vísceras do núcleo. Por ser neutra, penetra no núcleo sem sofrer a repulsão elétrica que barra a entrada de prótons e alfas. E, por ser relativamente pesada, consegue chacoalhar com eficiência o núcleo bombardeado. Era de se esperar, portanto, que nêutrons fossem mais adequados para produzir novos isótopos radioativos que as partículas alfas usadas pelo casal Joliot-Curie.

Enrico Fermi
Foi assim que, desde 1934, Enrico Fermi e seus ajudantes, na Itália, começaram a bombardear com nêutrons tudo que era núcleo existente, começando pelo núcleo do hidrogênio e seguindo adiante na tabela periódica do incrível Mendelyeev. Já a partir do flúor (Z=9), começaram a surgir novos isótopos radioativos. Ao chegarem aos elementos pesadões, como nosso querido urânio (Z=238), os italianos pensaram que estavam criando novos elementos artificiais, os transurânicos, com peso ainda maior.
Em 1935, Otto Hahn, Lise Meitner e Fritz Strassmann, em Berlim, resolveram repetir essas experiências que Fermi fazia na Itália. Como vemos, essa mania de arremedar os outros é uma prática comum em pesquisa. Pois vejam como o famoso fenômeno “Maria vai com as outras” também pode ocorrer no seleto clube dos cientistas: os alemães reproduziram as observações de Fermi e concordaram inteiramente com ele, inclusive na crença que estavam produzindo elementos transurânicos.
Irene e Frederico Joliot-Curie, na época em que os conhecí, estavam examinando as propriedades químicas dos elementos que obtinham bombardeando núcleos com nêutrons. Verificaram que as propriedades de alguns desses produtos das reações eram muito semelhantes às propriedades de elementos bem mais leves que o urânio. Se eles tivessem sido mais perspicazes (e audaciosos) teriam desconfiado que estavam, na verdade, quebrando os núcleos bombardeados em pedaços menores. As evidências estavam bem à frente de seus olhos – e dos meus, quando eles me contaram o que estavam fazendo – e ninguém se apercebeu do que era óbvio. Com isso, perderam outro prêmio Nobel.
A história é ainda mais impressionante pois, um ano antes disso, a química Ida Noddack, descobridora do elemento rênio, tinha sugerido que um nêutron poderia partir núcleos pesados em pedaços menores. Ninguém prestou atanção no que ela disse, nem ela mesma, pois não levou sua própria sugestão adiante.

Lise Meitner e Otto Hahn
Depois de tanto tiro no escuro, finalmente, em 1938, Hahn e Strassmann começaram a suspeitar que algo estranho estava acontecendo com os produtos das reações de núcleos e nêutrons que faziam em seu laboratório. Nessa época, Lise Meitner já estava na Suécia, fugindo de Hitler. Os alemães pediram ajuda à ex-colaboradora e ela, juntamente com seu sobrinho Otto Frisch, tiveram o estalo: a fissão nuclear tinha sido descoberta. Mas, essa história eu já contei.
(Veja LISE MEITNER E A FISSÃO NUCLEAR.)
Se você pensa que a comédia de erros e acertos da pesquisa nuclear nos anos 30 parou por aí, está enganado. Acontece que Fermi, ao bombardear núcleos, descobriu que nêutrons de baixa velocidade (os chamados “nêutrons térmicos”) penetram com mais eficiência no núcleo que nêutrons rápidos. A partir dessa observação, ele sempre fazia seu feixe de nêutrons passar por um “moderador”, antes de usá-los para bombardear amostras. O moderador pode ser uma fina placa metálica ou algum líquido ou sólido conveniente. Deu-se, alguns anos depois, que cientistas na Alemanha e nos Estados Unidos estavam loucos para descobrir qual o melhor material para servir de moderador em um reator nuclear ou, eventualmente, em uma bomba atômica. Na Alemanha, quem estava fazendo esses cálculos era o mesmo Walther Bothe que encontramos no início dessa história. Foi então que Bothe se estrepou: fez as contas erradas e concluiu que o melhor moderador era a chamada “água pesada”. A água pesada é a água normal (H2O) com os hidrogênios trocados por deutérios (D2O). Os alemães foram nessa onda e começaram a produzir água pesada, trabalho difícil, caro e demorado. Enquanto isso, Fermi, já nos Estados Unidos, concluiu que o grafite (esse mesmo que é usado em lápis) é muito melhor moderador, além de ser mais fácil de produzir.
Sorte da democracia ocidental: os nazistas nunca chegaram nem perto de fabricar uma bomba atômica. Até a fábrica de água pesada que tinham na Noruega foi destruída pelos ingleses em um famoso ataque aéreo e terrestre. Quanto ao velho Bothe: acabou também recebendo seu prêmio Nobel de Física, em 1954, pela invenção do “método da coincidência”, muito importante em medidas de física nuclear.
E aqui chega ao fim esse relato sobre a descoberta do nêutron e algumas de suas conseqüências. Hoje, os astrofísicos já sabem até que existem estrelas inteiras feitas de nêutrons. Uma estrela de nêutrons tem o tamanho de uma cidade como Sobral mas tem a massa de vários sóis. Ela pode girar, como a Terra gira, enviando sinais de rádio para o espaço. Esses sinais foram, pela primeira vez, recebidos por uma jovem inglesa, Jocelyn Bell, cuja história eu também já contei por aqui (Ver 100 Anos de Prêmio Nobel). Mais detalhes, fica para outra vez.

